- Появились вопросы?
- 8 (950) 128-05-60
- support@sibit3d.ru
Проект А. Д. А. М.

Технологическое планирование для пятиосевого аддитивного производства
30.01.2021
Руководство по 3D-печати. Материалы: пластики.
08.02.2021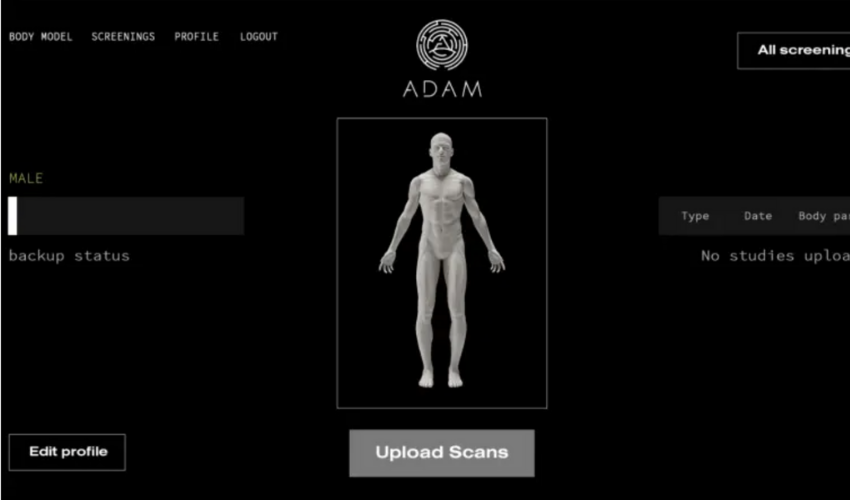
Основанная в 2018 году компанией 3D-печати Kwambio и компанией We Fund Ventures в Украине, компания ADAM разрабатывает костные имплантаты с 3D-печатью по требованию. Первоначальное видение компании состояло в том, чтобы создать инфраструктуру, подобную автомобильной мастерской, где любая часть человеческого тела могла бы рассматриваться как заменяемая деталь. В конце концов команда ADAM решила начать разработку проекта с акцента на костные имплантаты. Они разработали запатентованную технологию 3D-печати и композитные материалы для этих имплантатов (биополимерные и биокерамические материалы). Они показали, что первые прототипы прошли доклинические испытания на крысах линии вистар.
Решение, предложенное АДАМОМ, направлено на облегчение процесса хирургического планирования. На самом деле АМ все чаще интегрируется в рутину работы клинициста для оценки и разработки быстрых, индивидуальных и экономически эффективных решений для пациентов. Таким образом, пациенты могут загружать и безопасно хранить свои МРТ и КАТ-снимки на цифровой платформе ADAM. Когда пациент нуждается в костном имплантате, сертифицированные клиницисты могут использовать платформу для создания 3D-модели имплантата непосредственно на основе медицинских данных пациента.
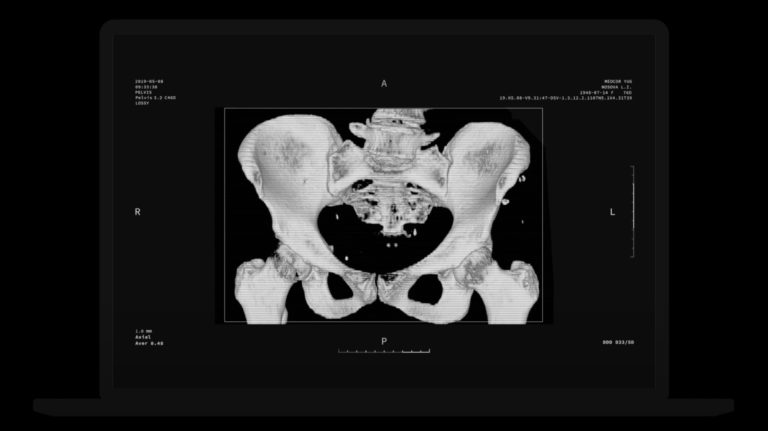
Затем 3D-модель костного имплантата конкретного пациента может быть использована для производства с использованием фирменных 3D-принтеров. Печать может осуществляться в ADAM или непосредственно на месте, в зависимости от предпочтений. Производство занимает около 24 часов, что значительно быстрее по сравнению с существующими альтернативами. Используемые композитные материалы также приводят к более низкой себестоимости производства, чем титановые или PEEK-имплантаты.
Сегодня команда ADAM объяснила, что успешные результаты испытаний позволили ей подать Q-представление в FDA. Программа Q-Submission FDA предоставляет заявителям возможность на раннем этапе сотрудничать и обсуждать заявки на медицинское оборудование. В своем ответе FDA подтвердило приемлемость ADAM biopolymer and bioceramic bone implants’ 510(k) – 510(k) требует демонстрации существенной эквивалентности другому легально продаваемому в США устройству.
Адам планирует завершить исследования на животных соответствии с требованиями FDA в 2021 году. Далее компания намерена получить нормативное разрешение на костные имплантаты и начать этап продаж в 2022 году. Костные имплантаты, однако, это только начало – в ближайшие годы АДАМ намерен начать исследования и разработки кровеносных сосудов, сердечных клапанов и бронхиальных имплантатов.